生きている細胞を無染色のまま、高速に画像化する誘導ラマン顕微鏡。そのスペックを大きく向上させて素早く動き回るミドリムシを画像化し、さまざまな環境下での物質代謝がミドリムシ個体間でどう異なっているかを、東京大学の研究グループが明らかにした。今回の成果により、例えば生産性の高い微生物個体を見つけ出すことが可能になるなど、さまざまなバイオ産業への応用が期待される。
―― 今回Nature Microbiology に発表された研究は、ImPACTプログラムの1つとして進めてこられましたね。

誘導ラマン散乱顕微鏡の実験室で。
合田氏: ImPACT(Impulsing Paradigm Change through Disruptive Technologies Program; 内閣府革新的研究開発推進プログラム)は、2014年に始まったプロジェクトで、発展性のある革新的技術の開発をめざし、ハイリスク・ハイインパクトな挑戦的研究開発の推進を目的にしています。その中で私のグループは、「セレンディピティ」の計画的な創出を目標にして、研究開発を進めてきました。
――セレンディピティの創出とは?
合田氏: セレンディピティとは、科学の世界でよく使われる言葉で、予期しない幸運な発見のことを指しています。こうした発見は、砂浜を探り一粒の砂金を見つけ出すような、偶然に頼る部分の大きいものと考えられています。我々は、その偶然の確率を格段に引き上げるシステムの開発をめざしているのです。
―― 具体的に、どのようなシステムなのでしょうか。
合田氏: 細胞を1つ1つ調べて、科学的および産業的に高価値な細胞を見つけ出す「細胞検索エンジン」の開発です。これまでのライフサイエンスにおける一般的な研究では、同じ種類の細胞であれば、細胞1つ1つの持つ個性というものは考慮せず、たくさんの細胞の平均値を用いて細胞の特性を評価していました。しかし、細胞には個性があり、ばらつきがあるということが多くの研究で明らかになってきています。そこで、細胞の個性を見分ける技術を開発できれば、同じ種類の細胞集団の中から、優れた能力を備えた個体や、未知の性質を示す個体を発見する効率を上げられるに違いないと考えました。
小関氏: 生物が進化したり、あるいは作物を品種改良したりするには、それなりの長い時間がかかります。この細胞検索エンジンを使えば、集団の中の優れた個体を探すことができるので、時間の大幅な短縮が可能になるはずです。
例えば、単細胞生物であるミドリムシ(Euglena gracilis)は、その代謝産物が産業に利用されています。脂質はバイオ燃料に、パラミロン(多糖)は健康食品に、といった具合です。もしミドリムシ集団の中から、生産能力の高い個体を見つけられたら、それを増殖させるなどして、生産能力の高い細胞集団を得ることができますよね。
誘導ラマン散乱顕微鏡のさらなる性能向上に挑戦
―― このシステムには、どのような技術が必要になるのでしょうか。
合田氏: いくつかの技術から成り立っていますが、今回の研究では、その要となる画像化装置の開発に取り組みました。生きている細胞1つ1つの挙動やその成分を高速に画像化するのが得意な顕微鏡として、誘導ラマン散乱(SRS)顕微鏡があります。SRS顕微鏡には細胞を染色せずに無標識で画像化できる、つまり無侵襲で観察できるという大きな特徴があります。しかも、それを非常に高速で画像化できるのです。
SRS顕微鏡の高速画像化が達成されたのは2012年のことで、これは、当時大阪大学にいた小関准教授たちの研究チームの成果です。今回我々の研究プロジェクトでは、この顕微鏡のさらなる性能向上を図ることを考えました。そして、1つの細胞内の分子の種類を同定したり、それを定量化したりできる計測装置の作製をめざしました。
―― SRS顕微鏡の原理を教えてください。
小関氏: 分子に光を照射すると、ラマン散乱光という微弱な光が発せられます。ラマン散乱光の周波数は、その分子の分子振動周波数によって決まり、分子振動周波数は、その分子の構造によって決まるので、ラマン散乱光の周波数と強度を計測すれば、分子の同定・定量ができます。これがラマン顕微鏡の基本原理です。これを改良して感度を上げたものが、SRS顕微鏡です。SRS顕微鏡では、分子に2色のパルス光を照射し、出力パルス光の強度の変化(誘導ラマン散乱効果)を検出します(図1)。
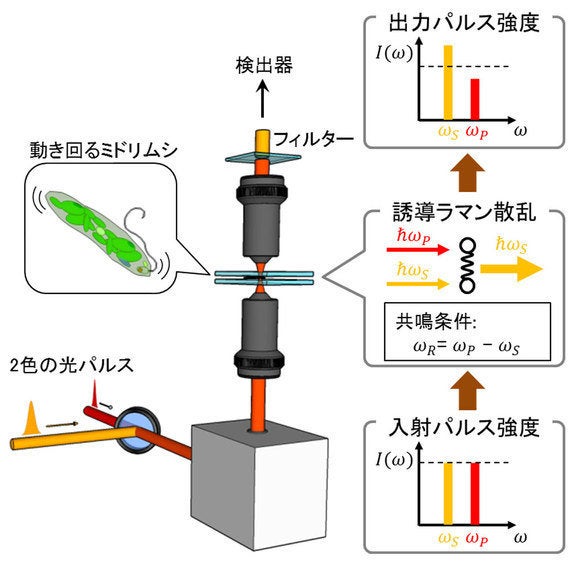
図1:誘導ラマン散乱顕微鏡の概念図
レーザーを用いて、2色のパルス光を対象物(動き回るミドリムシ)に照射する。出力パルス光の強度の差を検出して、対象物を同定する。パルス光の色(波長)は、見たい対象物に合わせてあらかじめ設定しておく。
このパルス光は、非常に強い光をごく短い時間照射できる特殊なパルスレーザーから発します。私が2012年に開発したものですが、5ピコ秒、つまり1兆分の5秒間だけ照射できる光源で、光の波長を高速で切り替える工夫を施してあります。
―― 高速で画像化できる「速い」顕微鏡には、どのような利点があるのでしょうか。
小関氏: 今回観察したミドリムシは非常に速く動き回るので、2012年の時点は画像化できず、装置のさらなる高速化が必要でした。つまり、高速で画像化できるということは、細胞の速い動きに対応できることにもなるわけです。
合田氏: もう1つ重要な利点として、画像化の高速化により、短時間で多くの細胞を観察できるようになることがあります。たくさんの細胞を比較すれば、より効率よく細胞の多様性を調べられ、高い精度でその個性を解析できるようになるはずです。
2012年の段階で、1秒間に約30コマの速さで画像化できていたのですが、今回、1秒間に110コマの速さまで高速化することに成功しました。
―― 今回、どのような点を工夫することで、さらなる高速化を達成されたのですか。
小関氏: 1つは、顕微鏡のデータの取り方を工夫したことです。ミドリムシを見るのに、顕微鏡の視野全部のデータは必要ありません。ミドリムシに限定した部分のデータのみを取るようにしました。
それから、もう1つ大事な点は、画像データの解析ですね。微生物の生体は主に炭素原子と水素原子から構成されていて、それらの互いの分子振動周波数はよく似ています。このため、ミドリムシから得られる分子振動周波数スペクトルから、各分子の成分を効率よく正確に抽出する方法が必要です。しかし、当初はその方法が分からず、苦労しました。
そこで、千葉大学の画像解析の研究チームに相談したところ、画像データの成分を分離する解析アルゴリズムを教えていただけました。それで、スペクトルから必要な成分を分離することができ、解析時間を圧倒的に短縮することができたのです。
動き回るミドリムシを画像化
―― SRS顕微鏡でミドリムシを画像化するまでの操作を具体的に教えてください。
小関氏: この顕微鏡では、見たい対象物の分子振動周波数を調べておき、それに合わせて顕微鏡を事前にチューニングしておく必要があります。我々は、ミドリムシに含まれる重要な成分である脂質、パラミロン、タンパク質、葉緑素を計測しようと考え、まず、これら4つを同定するための特徴的な周波数を、画像解析アルゴリズムを使って見つけました(図2)。その結果、4つの周波数で光の強度を計測すれば、これらの4成分を同定・定量できることがわかりました。こうしてチューニングし、生きているミドリムシをとらえた画像が図3です。
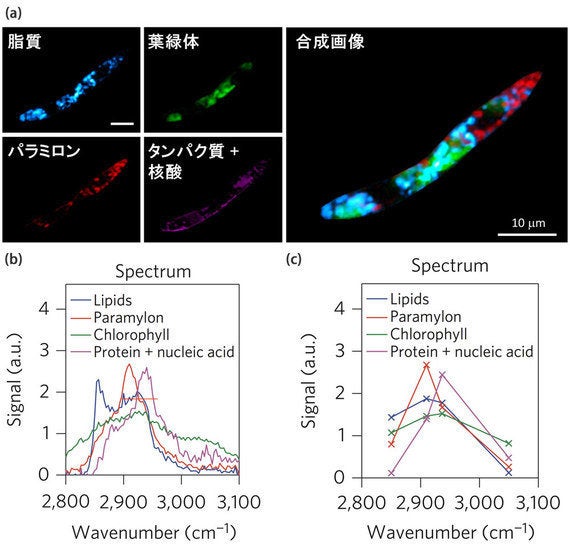
図2:ミドリムシの脂質やパラミロン分子を見るためのSRS顕微鏡のチューニング
固定したミドリムシ(a)を用いて、見たい分子別の出力パルススペクトルを得ておく(b)。このときに、不要なバックグランド成分から必要な成分を分離する画像アルゴリズムを用いる。4つの波長のみ測定すれば、脂質、パラミロン、葉緑素、タンパク質(+核酸)を見分けられることがわかった(c)。
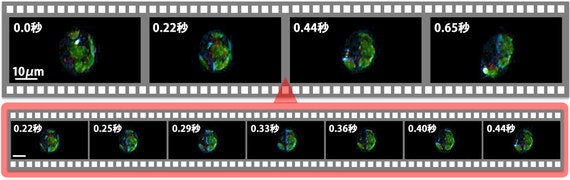
図3:動き回る生きたミドリムシを画像化
青、赤、緑でそれぞれ示されている脂質、パラミロン、葉緑素の合成画像。
―― ミドリムシの個性をとらえることはできましたか。
鈴木氏: 今回、100個体からなるミドリムシ細胞集団について、各ミドリムシ細胞内に含まれるパラミロン、脂肪、タンパク質、葉緑素を定量化し、比較することができました。その結果、各細胞における成分の量や細胞内分布にばらつきがあることがわかったのです(図4)。
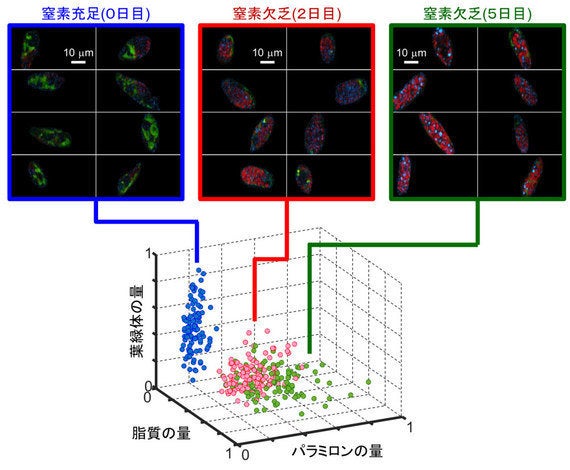
図4:窒素欠乏状態に置いたときのミドリムシ細胞の変化
上段はミドリムシのSRS像。下段は、各ミドリムシ細胞内部の脂質、パラミロン、葉緑素の成分量のばらつきを示すグラフ。下段の青、赤、緑は上段の0日目、2日目、5日目に対応する。
さらに、環境条件を変えたときの変化についても測定できました。窒素欠乏状態においた場合、各成分の変化には、細胞によってばらつきがありました。測定結果を統計的に解析すると、窒素欠乏状態ではパラミロンと脂質の量が増え、葉緑素の量が減ることがわかりました。
今回は、SRS顕微鏡を用いたファーストトライアルです。より充実した解析には、ほかの装置の開発も必要となります。
―― さらにどんな装置を開発される予定でしょうか。
合田氏: 現在、顕微鏡のステージに細胞を送り込む装置がまだ開発途上で、自動化できていません。今は、手作業で細胞を次々とステージにセットしています。ですから、顕微鏡の高速性を生かした連続的な画像化が、十分に実現できているとはいえないのです。現時点では、1回の実験で数百個の細胞しか画像化できていませんが、自動化できれば1分間以内に数千、数万という数を画像化できるようになります。
―― 手作業で100個体ものミドリムシ細胞を観察したのですね。
小関氏: 今回の研究はすべて、ポスドクの鈴木さんと大学院生の脇坂さんが実際の作業に当たってくれました。彼らの労力の結晶です。
脇坂氏: 同一環境条件で100個体ずつを観察するのですから、大変でした。顕微鏡の調整などにミスがあったりすると、また最初から計測を繰り返さなければなりませんでした。
―― 今回、投稿先としてNature Microbiology を選ばれた理由は?
合田氏: 実は、最初はNature Plants に投稿したのですが、エディターから、Nature Microbiology の方がふさわしいだろうとアドバイスいただき、トランスファーしました。我々の研究グループは、化学、物理学、工学、情報学などの専門家で構成されているのですが、生物学分野のジャーナルについては詳しくないので、ありがたかったです。
―― この顕微鏡で、他の微生物を画像化することもできますか。
合田氏: この方法を拡張していけば、いろいろなものに応用できます。
小関氏: どのようなことに適用すると生物学的意義があるのか、生物学者の方たちからぜひアイデアをいただきたいと思っています。
なお、見る対象物としては、ある程度密度が高くて凝集している物質である必要があり、水に溶けているような物質は苦手です。今回のパラミロンは、水にも油にも溶けず、蛍光分子が結合しないため、他の一般的な顕微鏡では見ることのできないものでしたが、SRS顕微鏡では非常に見やすい物質でした。
―― 今後、この研究をどのように展開されますか。
合田氏: 細胞を自動的にセットする装置をはじめ、システムを構成するその他の装置の完成をめざします。そして、ミドリムシやその他の微生物の個性を効率よく調べられるシステムに仕上げ、それらの産業利用を実用化していきたいと思っています。さらに、なぜその個性がもたらされているかをDNAやRNAレベルで調べ、スーパーな個体を作る「品種改良」を効率的に行って、低コストのバイオ燃料を開発したいとも考えています。また、微生物以外にも、例えば血液細胞などの観察からも、何か得られるものがあるのではないでしょうか。
―― ありがとうございました。
インタビューを終えて
インタビューの後に、SRS顕微鏡を見せていただきました。「現在はまだ研究用の手作りなので、大きいですよ」というその顕微鏡は、約2メートル四方の広い台の上にレーザー、コンピューター、ステージ台、無数のレンズなどが、所狭しと並んだものでした。レーザーから出た光は、たくさんのレンズで方向を変えられながら、綿密に調整されて(これが大変らしい)顕微鏡のステージ台へと向かうのです。将来は、メーカーによる小型化も予想されるとのこと。
Nature Microbiology 掲載論文
Brief Communication: 誘導ラマン散乱顕微鏡法を利用して、生きた微細藻類Euglena gracilisの代謝多様性を探索する
Nature Microbiology1 : 16124 doi:10.1038/nmicrobiol.2016.124 | Published online 1 August 2016
Author Profile
合田 圭介(ごうだ けいすけ)
東京大学大学院理学系研究科化学専攻 教授
2001年カリフォルニア大学バークレー校理学部物理学科 卒業
2007年マサチューセッツ工科大学理学部物理学科博士課程(米国)修了(Ph.D.)
2012年東京大学大学院理学系研究科化学専攻 教授(現職)
2013年カリフォルニア大学ロサンゼルス校工学部電気工学科(米国)兼任(現職)
2014年内閣府革新的研究開発推進プログラム(ImPACT)プログラム・マネージャー 兼任
小関 泰之(おぜき やすゆき)
東京大学大学院工学系研究科電気系工学専攻 准教授
1999年東京大学工学部電子工学科 卒業
2004年東京大学大学院工学系研究科電子工学専攻 博士課程修了(博士(工学))
2004年科学技術振興機構 博士研究員
2006年大阪大学生命先端工学専攻 助教
2009年科学技術振興機構 さきがけ研究者 兼任
2013年東京大学大学院工学系研究科電気系工学専攻 准教授(現職)
鈴木 祐太(すずき ゆうた)
東京大学大学院工学系研究科電気系工学専攻 日本学術振興会特別研究員
2009年大阪大学工学部応用自然科学科応用物理学科目 卒業
2014年ワシントン大学セントルイス校バイオエンジニアリング専攻(米国)博士課程修了(Ph. D.)
2015年東京大学大学院工学系研究科電気系工学専攻 日本学術振興会特別研究員(現職)
脇坂 佳史(わきさか よしふみ)
東京大学大学院理学系研究科化学専攻 博士課程
2014年東京大学理学部化学科 卒業
2016年東京大学大学院理学系研究科化学専攻 修士課程修了
2016年東京大学大学院理学系研究科化学専攻 博士課程入学
東京大学工学部プレスリリース

