次々と出る良好な実験データ─「うまくいきすぎて、怖いくらいでした」と、持田啓佑・大学院生は研究を振り返る。オートファジーは、細胞内の大規模分解システム。世界中で激しい研究競争が繰り広げられているこの分野で、細胞の小胞体に加え、核のオートファジーの仕組みをも明らかにすることに、わずか2年ほどで成功したのだ。
Nature 掲載論文
Nature 2015年6月18日号 Letter
受容体を介した選択的オートファジーが小胞体と核を分解する
doi:10.1038/nature14506
-- Natureダイジェスト:Natureに投稿したときは、博士課程1年目?
持田: はい。この研究は、大学院修士課程の1年目に開始しました。そのときは、まさか自分の研究がNatureに載るとは思ってもみませんでした。ところが実験を始めてみると、期待を上回る興味深い結果が次々と得られて、なんだか怖いくらいでした。
-- この研究テーマのきっかけは?
大学4年生のときに中戸川仁先生の研究室でオートファジー(自食作用)の研究を始めましたが、最初に選んだテーマはあまりうまくいかなくて......。それで、修士課程に進むときに新しいテーマをいろいろ考えて、小胞体のオートファジーに関わる未知の分子を探したいと申し出ました。中戸川先生も、面白そうだねと賛成してくださったので、先生に相談しながら研究を進めてきたのです。
-- なぜ小胞体に着目されたのですか。
オートファジーは、細胞内の不要な成分や有害な成分を分解する作用です。分解の対象にはタンパク質などの物質ばかりでなく、ミトコンドリアなどの細胞小器官(オルガネラ)も含まれることが、近年の研究により明らかになってきました。
現在、さまざまな細胞小器官について、オートファジーとの関連が盛んに研究されています。小胞体は、タンパク質や脂質の合成などを担う重要な細胞小器官です。オートファジーが小胞体を積極的に分解していることは報告されていましたが、小胞体を選んで分解するメカニズムは分かっていませんでした。
標的が選択的に分解される仕組み
-- オートファジーはどのような過程で起こるのですか。
特別な膜ができて、分解の対象物を包み込み、オートファゴソームと呼ばれる小胞を作ります。これが細胞内の"分解の場"に輸送されて、酵素により分解されるのです。分解の場とは、酵母や植物細胞の場合は液胞、動物細胞の場合はリソソームです。
-- 分解する対象を選ぶ仕組みは?
分解対象を選択できるのは、目印となるタンパク質(オートファジー受容体)が対象物上に存在しているからだと分かっています。対象物を包む膜上のAtg8というタンパク質がこの目印に結合することで、対象物を選択できるのです。オートファジー受容体は、対象物の種類ごとに異なっていて、ミトコンドリアやペルオキシソームに特有な受容体がすでに発見されています。
小胞体の受容体を網羅的に探す
-- どのように研究を進めましたか。
研究を始めた当初は、小胞体の選択的オートファジーにおいても分解の目印となるオートファジー受容体が存在するのかどうかが不明でした。中戸川研究室で実験材料としている出芽酵母を用いて解析を進めた結果、Atg8と結合するタンパク質の中に小胞体のオートファジーの受容体が存在することを確信しました。Atg8の機能を部分的に欠損させると、小胞体のオートファジーが低下したからです。
そこで、受容体の探索に着手しました。具体的には、Atg8と結合するタンパク質を質量分析で網羅的に同定する方法をとりました。質量分析は、横浜市立大学の平野久教授にお願いしました。
平野先生から質量分析の結果が返ってきたのが2013年の12月です。その結果をもとに受容体の候補を9つに絞り込み、実験で確認することにしました。小胞体に局在するかどうか、そして、そのタンパク質を欠失させると小胞体の分解が止まるかどうかを調べたのです。
その結果、Atg39とAtg40と名付けた2つのタンパク質が探し求めていた受容体と分かりました。質量分析をしても目的のタンパク質を同定できないこともありますので、1回の分析で目的のタンパク質を同時に2つも同定できたのは幸運でした。
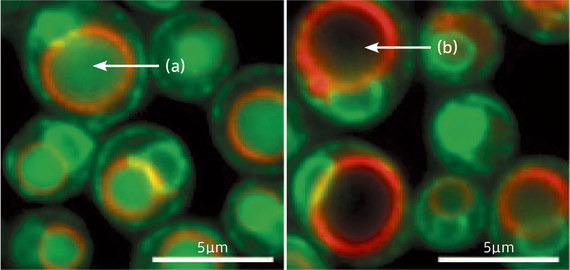
左は酵母の野生型細胞、右はAtg39と40の変異体。赤色は液胞の周囲の膜、緑色は小胞体の膜タンパク質を示す。飢餓条件下では小胞体の分解が起こるが(液胞の内部(a)が緑色になることで分かる)、Atg39とAtg40を両方欠損させると分解は起こらない(液胞内部は暗黒色(b))。
-- 小胞体にはオートファジー受容体が2つもあるのですね。
そうなのです。出芽酵母の細胞内で小胞体が存在する場所は主に3カ所で、1)核の周囲、2)細胞質、3)細胞膜の直下です。Atg39は1)の核の周囲の小胞体に主に存在してその分解の目印となり、Atg40は2)細胞質や3)細胞膜直下の小胞体に多く存在してその目印となることが分かりました。2つのオートファジー受容体が、それぞれの小胞体領域の分解に特化しているという事実には驚きました。
核のオートファジー受容体が見つかる
-- Atg39は核の受容体でもありますね。
はい。ただし、当初は、核の周囲に存在する小胞体のみが分解されるのだと思っていて、核の内容物まで分解されるとは予想していませんでした。
あるとき、電子顕微鏡でオートファゴソームに取り込まれた小胞体を観察してみると、Atg40を受容体とするものとAtg39を受容体とするものとでは、形態が異なっていました。Atg40に対応するものはチューブやシート状の小胞体で、Atg39に対応するものはリング状の小胞体でした。そして、リングの内部は細胞質ではないように見えたので、何が入っているのかと不思議でした。
-- リング状の内部は何なのでしょう?
中戸川先生が、「もしかしたら核だったりしてね」とおっしゃいました。僕は、まさかとは思いましたが、調べてみると、なんと、本当に核の内容物だったのです。ウェスタンブロット法や免疫電子顕微鏡解析で得られた画像には、リングの内部に核のタンパク質が含まれていることが示されていました。このときは、本当にびっくりでした。すぐには信じられないくらい。その晩は、興奮してなかなか寝付けませんでした。
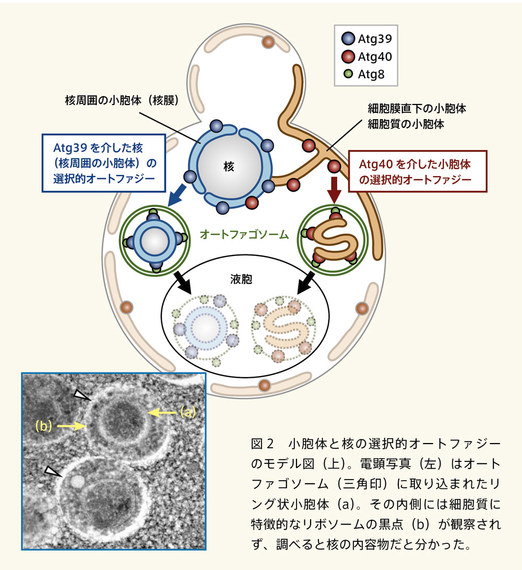
図2 小胞体と核の選択的オートファジーのモデル図(上)。電顕写真(左)はオートファゴソーム(三角印)に取り込まれたリング状小胞体(a)。その内側には細胞質に特徴的なリボソームの黒点(b)が観察されず、調べると核の内容物だと分かった。
投稿するジャーナルが決まる
-- Natureに投稿と決めたのはいつ?
核に関する結果が出た頃から、中戸川先生とトップジャーナルへの投稿を検討していました。
また投稿の半年ほど前の2014年夏、海外の学会で中戸川先生がゲーテ大学(ドイツ)のIvan Dikic博士と偶然お話をされ、そこでDikic博士が「哺乳類で小胞体のオートファジー受容体を見つけたので、タイミングが合えば一緒に投稿しよう」と提案されたそうです。しばらくしてDikic博士から、「自分たちはNatureに投稿するが、1カ月以内に論文をまとめて一緒に投稿できるか?」とメールが来ました。この機会を生かした方がよいだろうと、中戸川先生と話し合って、急遽論文をまとめてNatureに投稿し、同時掲載となりました。
-- 論文をまとめられて......。
メールを受け取ったとき、こちらはまだ論文をまとめる準備をしていなかったので、同時に投稿するためには研究を急がなくてはなりませんでした。僕としては、小胞体と核の選択オートファジーが、生理的にどんな意味を持つのかも調べようと思っていました。生理的に意味のない現象だったら、発見したことの価値も薄れてしまいますから。
基本的な解析しかできませんでしたが、栄養状態が悪い飢餓時の細胞の生存にこれらのオートファジーが重要であることが分かりました。最後は技術員の方にも手伝ってもらって何とか投稿までこぎつけました。
-- 投稿、アクセプトと、どのようなお気持ちですか。
投稿後、エディターからの返事は安心できるもので嬉しかったのですが、どのタイミングで喜べばいいのか分かりませんでした(笑)。万が一ダメだったらと、2回のリバイスを経てアクセプトの返事をもらうまで、喜ぶのをずーっと抑えていたのです。そうしたら、何だか、本格的に喜ぶタイミングを逸した気がします。
今後は、今回の発見の生理的な意味を、もっときちんと探っていきたいと思います。また、Dikic博士の論文では、哺乳類の小胞体のオートファジー受容体が、ヒトの神経疾患と関連することが報告されています。この受容体の構造は酵母のAtg40に似ているので、その点も調べていきたいと思っています。また、オートファゴソームに小胞体や核の一部が取り込まれる過程にも謎がまだ多いので、今後明らかにしていきたいです。
Author Profile
持田 啓佑(もちだ・けいすけ)
東京工業大学 大学院生命理工学研究科
生体システム専攻 形態形成学分野
2013年 東京工業大学生命理工学研究科卒業
2014年 東京工業大学大学院修士課程修了(生体システム専攻形態形成学分野)
指導教官インタビュー
ダイナミックな膜の動きに魅せられて
中戸川 仁
東京工業大学 大学院 生命理工学研究科 生体システム専攻 形態形成学分野 准教授
-- オートファジーでは、単なる物質ばかりでなく、複雑な構造体まで分解されるのですね。
生物が生きていく上では、必要なものを作るばかりでなく、不要になったものを壊す作用も必要です。その分解システムの1つがオートファジーです。細胞小器官のような複雑な構造体の分解には適していると感じます。複雑な構造体でも膜で包んで"分解の場"である液胞やリソソームに放り込めば、そこにある何種類もの酵素が分解してくれますから。
-- 選択的オートファジーと非選択的オートファジーの違いは?
今回の論文は、特定の対象物を狙って分解する「選択的オートファジー」について研究したものです。オートファジーには、この他に、細胞内の成分を無作為に分解する非選択的な方法があります。選択的オートファジーは比較的最近発見されました。生理機能や病気と関連することが多いためか、盛んに研究されています。
-- 今回、核のオートファジーが見つかって驚かれましたか?
そうですね。とはいえ、これから詳しいメカニズムを解明していく必要があります。例えば、核にはDNAが含まれていますが、それを分解してしまったら細胞はおそらく死んでしまうでしょう。DNAを避けながら核の一部だけをどうやって分解するのか大変興味深いです。
また、Atg40とヒト疾患は関連しそうですが、核の受容体であるAtg39に対応する哺乳類のタンパク質についてもこれから調べていきたいと考えています。
-- オートファジーに興味を持ったきっかけは?
私がオートファジーに最初に興味を持ったのは、学会で大隅良典先生の講演を聞いたときです。膜が伸びていって、分解する対象物をぱくっと食べるように包み込む、そのダイナミックなイメージに惹かれ、オートファジーの過程で膜が作られる仕組みを明らかにしたいと思いました。これは今も私のメインテーマです。
その後、2004年に基礎生物学研究所の大隅研究室に博士研究員として加わり、オートファジーの研究を開始しました。2009年には、大隅先生と一緒に東工大に移り、2014年に独立しました。
-- 学生の指導で心掛けているのは?
学生自身が興味を持って楽しんで研究を進めることの大事さが、持田君を見ていてよく分かりました。持田君が提案したテーマは、他の研究チームとの競争になる可能性が大いにありました。しかし一度始めたら、彼はどんどん自分で調べて、短期間で大きな成果を挙げてくれました。その過程で研究者としても大きく成長したと思います。本人が夢中になれることが大切なのですね。研究の楽しさを伝えるためにも、例えば学生が私と気軽に話せる環境を維持することが重要だと思っています。
オートファジーの開拓者
誰も注目しなかった液胞でオートファジーを発見
大隅 良典
東京工業大学フロンティア研究機構 栄誉教授
-- 2015年3月に、オートファジーの仕組みの解明でガードナー国際賞を受賞されました。おめでとうございます。
酵母を使い、液胞の観察をもとにオートファジーを発見したのは、1988年のことです。東京大学で助教授として初めて自分のラボを持った年でした。最初は私1人。後になってポスドクの方が1人加わってくれた、小さなラボでした。そこでの8年間の研究が私の原点です。
-- 研究のライバルはいたのですか。
酵母は優れたモデル生物であり、大勢の人たちに研究されていましたが、液胞だけは別でした。細胞のゴミ溜めのように思われていたので、ほとんど注目されることもなく、競争も比較的少なくて、私はじっくり研究することができました。
酵母でオートファジーの現象を発見したので、その様子を電子顕微鏡で解析することにしました。時間依存的な過程を電顕で撮影するのですから、簡単な作業ではありません。素晴らしい電子顕微鏡技術を持っている馬場美鈴(ばばみすず)さんとの共同研究が始まりました。論文発表では手間取りましたが、他の研究者がすぐに迫って来ることができなかったのは、この「優れた電顕写真を撮影する」という壁が存在したからかもしれません。
-- オートファジーに関与する遺伝子も発見されたのですね。
遺伝子についても、オートファジーに関する遺伝子はほとんど注目されていませんでした。当時、研究者が注目していたのは「生存に必須の遺伝子」で、オートファジーに関与する遺伝子は必須遺伝子ではなかったので、誰も相手にしなかったのです。ですから、私たちはかなりの数の遺伝子を発見することができました。オートファジーは、飢餓という条件にしたときに初めて見えてくる現象で、オートファジー遺伝子は栄養培地での増殖には必須ではないのですが、オートファジーがおかしくなると、細胞は生存できなくなり、動物はさまざまな病気になってしまうのです。
-- 論文掲載では、苦労されたということですが。
私が力不足だったこともあるでしょうし、エディターと喧嘩する術も知らなかったので、論文掲載まですったもんだしました。Journal of Cell Biology に最初の論文が掲載されたのは、投稿2年後の1992年のことです。おかげで、その2年間に遺伝子の同定も済ませることができ、翌年にはすぐに遺伝子の論文も発表できました(笑)。
そのときの経験などから、私が最近のジャーナルに少々不満なのは、新しい発見をしたということをなかなか認めてくれないことです。どのジャーナルのエディターも、まず、「形態の報告にすぎない」「メカニズムについて触れておらず、単なる現象論だ」などと評します。仕方のないことかもしれませんが。でも、新しい現象の発見で、いきなりメカニズムまで解明できるはずがありません。ですから、とにかく発表できるところに発表することが大事だと思います。よい仕事には、必ず後から評価がついてくるはずです。