1――がんの治療法
1|日本では、がんが死因の第一位を占めています
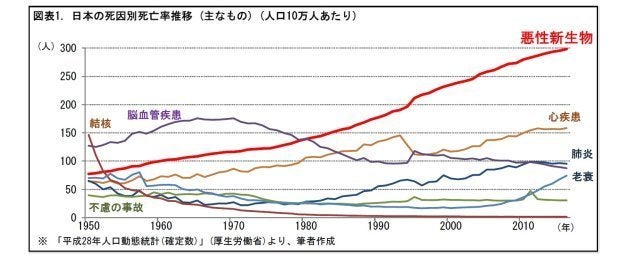
日本では、1981年以降、がんが死因の第1位を占めています。世界的にみても、がんは先進国で主要な死因の1つとなっています。このため、がんの診断法、治療法や、抗がん剤について、世界中の医療研究機関で、精力的に研究が進められています。がんの治療法について、見ていきましょう(*1)。
(*1) 本稿は、「がん情報サービス」(国立がん研究センター)、「明解医薬品産業」漆原良一 (医薬経済社, 2014年12月)、「薬事ハンドブック2018」(じほう) 、「すごいバイオ薬 オプジーボに続け! がん治療に高まる期待」(毎日新聞出版, 週刊エコノミスト2016年12月6日号)などを参考に、執筆しています。
2|外科手術、放射線治療、抗がん剤治療が、がんの主な治療法です
がんは、以前から多くの治療法の研究が進められており、がん患者の生存率向上に寄与してきました。がんの治療法の主なものは、外科手術、放射線治療、抗がん剤治療の3つです。これらは、併用されることも一般的です。
がん組織が切除可能であれば外科手術による組織の除去、切除が困難な部位にあれば放射線治療や抗がん剤治療が行われます。また、高齢患者で身体にかかる負荷の面から外科手術が困難な場合に、放射線治療や抗がん剤治療が行われることもあります。更に、外科手術や放射線治療を行った後に、再発を予防するために、抗がん剤を投与する治療法(アジュバント療法)も一般的に行われています。

(1) 外科手術
外科手術として、従来より、開腹手術が行われています。最近は、口や肛門から内視鏡を挿入して行う内視鏡手術や、患部の周辺に穴を開けてそこから腹腔鏡を挿入して行う腹腔鏡手術が増加しています。開腹手術に比べて、患者の身体面の負担が小さく、術後の回復も早いことが普及の背景にあるものとみられます。
手術支援ロボット「ダヴィンチ」を使う、内視鏡手術の利用も進んでいます(*2)。ロボットの利用により、体内深部での精緻な器具操作が可能となっています。前立腺がんと腎臓がんに続き、2018年度には、肺がん、食道がん、胃がん、直腸がん、膀胱がんなど、新たに12件の手術が保険適用となりました。開腹手術が行えない高齢患者に対する手術として、注目度が高まっています。
(*2) 「ダヴィンチ」は、"da Vinci Surgical System"(インテュイティブ サージカル社)の通称。
(2) 放射線治療
放射線治療では、X線、ガンマ線、電子線、陽子線、重粒子線などが治療に用いられます(*3)。これらを照射して、遺伝子を傷つけてがん細胞の分裂・増殖を阻害したり、がん細胞が自ら脱落する現象を増強したりします。
体の外部から放射線をあてる、外部照射が一般的です。放射線物質を体内に挿入したり、薬として服用したり、注射で投与する内部照射が行われることもあります。
外部照射では、病巣に多方向から放射線を集中させることで、ピンポイントで高線量の放射線をあてる定位放射線治療が行われるようになっています。これにより、周囲の正常組織にあたる線量を極力減少させることや、患者の治療回数が減って通院の負担が軽減することが期待されています。
なお、陽子線治療や重粒子線治療では、保険適用となるがん以外に、先進医療として臨床試験が行われるものもあります。この場合、先進医療分の治療費は全額患者負担で、健康保険の高額療養費制度も適用されません。このため、治療費の面で、患者の負担は大きくなります。
(*3) 陽子線は、水素の原子核ビーム。重粒子線は、主に炭素線イオン。
(3) 抗がん剤治療
抗がん剤治療は、薬剤を投与して、がんの増殖を阻害したり、がん細胞のもつ特定のタンパク質を標的にしてがん細胞を攻撃したりする治療法です。
抗がん剤治療の技術は、画期的な効果を示す医薬品や再生医療等製品の研究・開発が進められており、近年、目覚しく進歩しています。現在、本格的に治療に用いられているのは、化学療法剤、分子標的薬、免疫チェックポイント阻害剤です。
以下、抗がん剤治療について、見ていきましょう。
①化学療法剤
化学療法剤は、日本では第2次大戦後間もなく開発され(*4)、その後、進化を続けています。DNAの複製や細胞分裂を阻害することにより、がん細胞の増殖を抑えることができます。
しかし、化学療法剤には、副作用もあります。がん細胞のような増殖スピードの速い細胞に作用するため、例えば血液中の白血球が減少して免疫力が落ちたり、毛髪細胞が影響を受けて毛が抜け落ちたり、胃の中の細胞に影響して吐き気を誘発したりします。
②分子標的薬
分子標的薬は、がん特有の分子を標的に増殖を抑制します。がん細胞の特徴を認識した上で、その増殖や転移を行う特定の分子だけを狙い撃ちにします。このため、正常な細胞へのダメージが少なくなります。副作用が全くないわけではありませんが、化学療法剤に比べると、患者の負担は小さくなります。
ただし、分子標的薬は、すべての患者に効くわけではありません。そこで、患者の遺伝子を調べて異常がある遺伝子を特定し、それに応じて分子標的薬を選択する、がんゲノム医療が始まっています。
2018年4月現在、全国で、がんゲノム医療中核拠点病院として11施設、がんゲノム医療連携病院として100施設が指定されています(*5)。連携病院は、患者のがん組織を中核病院に送って遺伝子検査を依頼し、その結果をもとに治療を行うこととなります。
また、分子標的薬は、投与を続けていくとがん細胞に耐性が出て、薬が効かなくなることがあります。これまでにさまざまな分子標的薬が登場して治療の選択肢が増えており、耐性の問題への対応が進められています。分子標的薬は、注射剤の抗体医薬と、経口剤の低分子薬とに分けられます(*6)。
③免疫チェックポイント阻害剤
免疫チェックポイント阻害剤は、体内の免疫機構を活性化させて、がん細胞を攻撃して死滅させます。抗体医薬のひとつで、分子標的薬の中に位置づけることができます。
近年、画期的な効果を示す免疫チェックポイント阻害剤が登場しています。免疫チェックポイント阻害剤は、2014年にオプジーボ(小野薬品工業社)が発売されたのが最初です(*7)。
通常、がん治療の効果をみる際の指標として、5年生存率が挙げられます。免疫チェックポイント阻害剤は、これから投与後5年を迎える患者が出現することとなりますので、その効果の持続性に注目が集まっています。
実際の抗がん剤治療では、化学療法剤と分子標的薬を併用する併用療法や、これに免疫チェックポイント阻害剤も併用する3併用療法などが行われています。
(*4) 第2次大戦中に使われた化学兵器の毒性を弱めたものとして、ナイトロジェンマスタードN-オキシド (商品名 ナイトロミン) が開発され、1950年代に販売されました。なお現在、同薬は日本では販売されていません。
(*5) 2018年4月時点で岩手、群馬、大分、熊本、沖縄県には、連携病院はありません。今後、半年ごとに厚生労働省への追加応募の受付が行われる予定となっています。
(*6) 注射剤として、アバスチン(中外製薬社)、ハーセプチン(同)、リツキサン(全薬工業社、中外製薬社)、ベクティビックス(武田薬品工業社)、ベルケイド(ヤンセンファーマ社、武田薬品工業社)、などが国内で承認されています。また、経口剤として、レブラミド(セルジーン社)、スプリセル(ブリストル・マイヤーズ スクイブ社、大塚製薬社)、グリベック(ノバルティスファーマ社)、タシグナ(同)などが国内で承認されています。
(*7) 2018年1月時点で、オプジーボ(小野薬品工業社)、キイトルーダ(MSD社)、ヤーボイ(ブリストル・マイヤーズ スクイブ社)、バベンチオ(メルクセローノ社・ファイザー社)、テセントリク(中外製薬社)が、国内で承認されています。
2――がんの新たな治療法
現在、次世代のがん治療法として、さまざまな研究や開発が進められています。特に、急ピッチで進められているのが、ペプチド医薬、遺伝子治療、ウイルス療法、核酸医薬、ワクチン療法です。
1|ペプチド医薬は、がん細胞内に入り込んでタンパク質の結合を阻害します
ペプチド医薬は、分子量が低分子薬と抗体医薬の間にあり、中分子医薬に位置づけられます(*8)。抗体医薬よりも分子量が小さいので、がん細胞内に入り込むことができます。
一方、低分子薬よりも分子量が大きいので、低分子薬にはできないタンパク質の結合阻害が可能となります。つまり、低分子薬と抗体医薬の長所を兼ね備えた医薬品といえます。ペプチド医薬は、経口投与が可能で患者の負担が軽いため、高齢患者への投与に向いています。また、製造コストが安く済むことも期待されています(*9)。
(*8) ペプチドとは、2個以上のアミノ酸分子が、一方のアミノ基(化学記号では、-NH)と他方のカルボキシル基(同、-COOH)とから1分子の水がとれて結合 (同、-NHCO- (ペプチド結合))した化合物をいいます。明確な基準がある訳ではありませんが、分子量は、低分子薬は100~300、抗体医薬は15万程度であり、ペプチド医薬はこの間の500~6,000程度となります。
(*8) リューブリン(武田薬品工業社)が国内で承認されています。
2|遺伝子治療は、免疫細胞の遺伝子を組み替えて、がん細胞を攻撃します
遺伝子治療は、がん細胞に特有の抗原に反応する遺伝子を人工的に作り、体内から取り出した免疫細胞に組み込みます。この免疫細胞を体内に戻すと、がん細胞への攻撃を行なうこととなり、がん治療を進めることができます(*10)。
多くの医薬品メーカーが開発に力を入れています。これまでに、白血病やリンパ腫など血液がんに対して臨床試験が実施され、治療効果が報告されています。今後、固形がんに対して効果を発揮する遺伝子治療の研究・開発が進められる見通しです。
(*10) キメラ抗原受容体T(CAR-T)細胞療法と呼ばれています。
3|ウイルス療法は、体内でがん細胞に感染するウイルスを用いて攻撃します
ウイルス療法は、がん細胞だけに感染してがんを破壊するウイルスを用います。ウイルスの遺伝子を組み替えて、正常な細胞に対しては機能せず、がん細胞だけを攻撃するようにして、体内で感染させて治療を行います(*11)。
従来の治療法(外科手術、放射線治療、抗がん剤治療)と併用することが可能で、いくつかの療法について、臨床試験が開始されています。
(*11) 医薬品として、IMLYGIC(アムジェン社)がアメリカやヨーロッパで承認されています。この医薬品は、国内未承認です。
4|核酸医薬は、リボ核酸 (RNA) を標的にして、がん細胞のタンパク質合成を阻害します
核酸医薬とは、デオキシリボ核酸(DNA)やRNAといった細胞内の遺伝情報を司る物質である核酸を医薬品として利用するものです。従来の抗がん剤がDNAから作られるタンパク質を標的にしている一方、核酸医薬はメッセンジャーRNA(遺伝情報をタンパク質の生合成装置に伝える働きを持つ)などの細胞内のリボ核酸を標的とします。
分子量の面で、ペプチド医薬と同様、中分子医薬に位置づけられます。核酸医薬は、生体内で分解されやすいのが難点で、体内での運搬技術の研究が進められています。
5|ワクチン療法は、ペプチドワクチンを注射してがんを攻撃するリンパ球を作り出します
ワクチン療法では、まずがん細胞の表面に、免疫細胞にとって攻撃の目印となるペプチドを見つけ出します。そして、そのペプチドを人工的に作って、ワクチンとして体内に注射します。
体内では、免疫細胞が、注入されたペプチドを外敵(異物)と認識して、キラーT細胞と呼ばれるリンパ球(*12)を大量に作ります。このリンパ球が、がん細胞を攻撃していきます。ワクチン療法は、がんを患者の免疫に認識させて攻撃を促す形で治療につなげていきます。
(*12) リンパ球は、白血球の成分の一種で免疫を行います。NK細胞、T細胞、B細胞があります。
3――がん治療にかかる費用
治療にかかる費用は、がんの種類、治療方法、使用する抗がん剤などによって異なります。ここでは、一例として、厚生労働省の公表データをもとに費用を見てみることにします。ひと月の平均的な費用を筆者が試算したところ、次のようになりました。
実際に、がん治療を行う場合は、まず主治医の説明をよく聞きます。その上で、治療効果、副作用、治療費等を十分に検討して、主治医とよく相談をしながら治療方法を決めていく必要があります。
関連レポート
(2018年4月16日「基礎研レター」より転載)
株式会社ニッセイ基礎研究所
保険研究部 主任研究員