
1――ジェネリックとは
近年、ジェネリックや後発医薬品という言葉を、メディア等で見かける機会が多くなっています。ジェネリックとは、どういう医薬品なのでしょうか。
1|医薬品は、新薬、長期収載品、ジェネリック(後発薬)の3つに分けられます
通常、医薬品を製造したメーカーは、特許を取得します。特許期間中、その医薬品の販売を独占することで、医薬品の製造コストを賄い、収益をあげることが可能となります。
医薬品は、特許の面から、新薬、長期収載品、ジェネリック(後発薬)の3つに分けることができます。新薬は発売から5~10年程度の間、特許を伴って、独占的に販売されます。
長期収載品は、新薬の特許が切れた後に、薬価基準に収載されたままになっている医薬品を指します。そして、ジェネリック(後発薬)は、新薬と同様の薬効をもつ医薬品で、特許の切れた新薬からの置き換えを狙って、新薬よりも低価格で市場に投入されるものを指します。
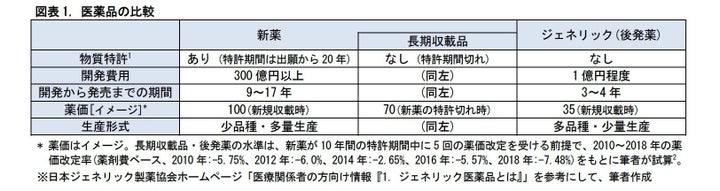
(*1) 有効成分の特許のことで、この他に製法特許(製造方法の特許)、用途特許/医薬特許(効能効果の特許)、製剤特許(用法用量の特許)があります。通常、特許出願は臨床試験の前に行われます。その後の開発・審査に10~15年かかるため、発売から5~10年程度で特許期間切れとなります。なお、製薬会社が申請すれば、5年を上限に特許期間の延長が認められます。
(*2) この試算では、後発薬の新規収載時の薬価は、長期収載品の5割としています。算定ルール上、後発薬の新規収載時は新薬の5割 (内用薬で収載希望品目数が10を超える場合は4割)で算定します。新薬が新薬創出・適応外薬解消等促進加算の対象の場合、加算分を差し引いた薬価から算定します。バイオ後発薬の場合は、上述の5割を7割、4割を6割とそれぞれ読み替えて算定します。
2|日本はジェネリックへの切り替えが進んでいません
欧米では、医師による、有効成分の一般名での処方が浸透しており、新薬の特許が切れると、速やかに後発薬に切り替えられるため、長期収載品の使用はほとんどありません。
一方、日本では、従来、ジェネリックへの切り替えの必要性が十分に浸透しておらず、特許が切れた後でも、長期収載品が、そのまま使われ続けることが多い傾向にありました。近年、このことが、医薬品費用が増大する要因の1つとして、挙げられてきました。
3|抗体医薬として、分子量の大きいバイオシミラーの開発が進められています
医薬品は、端的に言えば、多数の分子からなる化合物です。従来からある薬は、主として、低分子薬です。これは、主に経口剤として、化学合成で作られます。この低分子の新薬に対する後発薬は、新薬と有効成分が同じで、同一の効能を示すものとなります。
近年、これとは別に、生物学的製剤が開発されるようになりました。生物学的製剤は、製造過程で、生体由来の物質や、発酵・培養といった生物の機能を使って作られるもので、主に、注射剤として開発されます。
後発薬として開発しても、発酵や培養の際の温度等の条件が異なるため、新薬と全く同じ内容の医薬品ができる訳ではありません。このため、類似品を表す「シミラー」という用語を用いて、「バイオシミラー」とも呼ばれています。
バイオシミラーは、これまでタンパク製剤の開発が中心でしたが、がんやリウマチなどの抗体医薬として、分子量の大きな医薬品の開発が進められています。
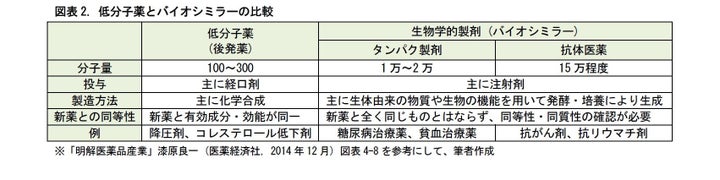
バイオシミラーは、低分子の後発薬と異なり、培養棟などの大がかりな開発設備を必要とします。このため、ジェネリック専業メーカーよりも、むしろ新薬メーカーの方が手がけやすいと考えられます。現在、大手新薬メーカーや、その関連のベンチャー企業を中心に、開発が進められています。
2――ジェネリック推進の動き
医療費削減に向けた取り組みの1つとして、ジェネリックの使用を推進する動きが始まっています。
1|政府は、2020年9月までに、後発医薬品の使用割合を80%にする目標を示しています
政府は、ジェネリックの普及等に向けて、数値目標を示しています。「経済財政運営と改革の基本方針2017」(骨太の方針)では、2020年9月までに、後発医薬品の使用割合を80%とし、できる限り早期に達成できるよう、更なる使用促進策を検討する。
バイオ医薬品及びバイオシミラーの研究開発支援方策等を拡充しつつ、バイオシミラーの医療費適正化効果額・金額シェアを公表するとともに、2020 年度末までにバイオシミラーの品目数倍増(成分数ベース)を目指す。など、とされています。
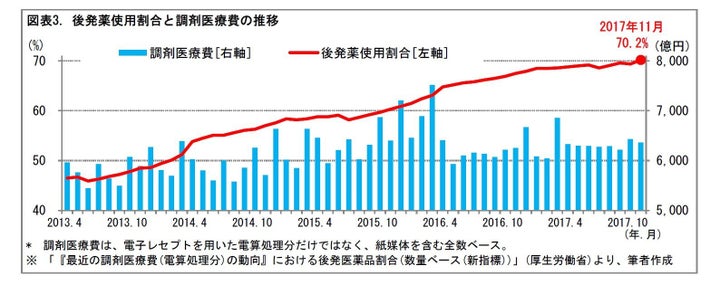
2|後発薬使用割合は徐々に上昇し、2017年11月には70.2%に達しています
実際に、後発医薬品の使用割合は、徐々に上昇しています。2017年11月には70.2%に達しています。その効果もあるのか、2016年度以降、毎月の調剤医療費の金額は以前よりも抑制的に推移しています。
3|ジェネリック普及のために、診療報酬での促進などが進められています
ジェネリック普及の背景には、いくつかの要因が挙げられます。診療報酬による促進、品質確保の取り組み、安定供給体制の整備です。
(1) 診療報酬による促進
診療報酬上、後発薬を処方、調剤するための加算項目などが規定されています。これらの規定が、保険薬局や医療機関に、後発薬使用を促す要因となっているものと見られます。
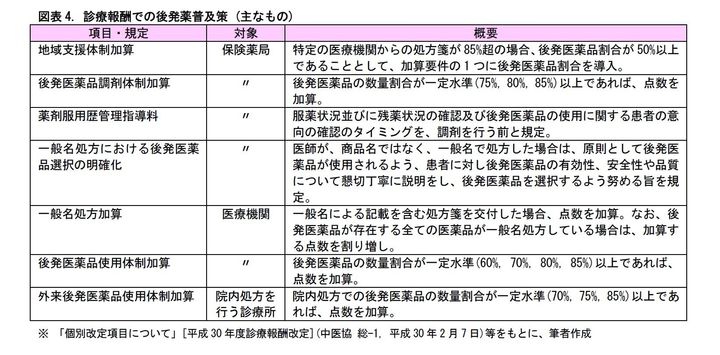
(2) 品質確保の取り組み
厚生労働省では、ジェネリックの品質に関して、各種学会での発表や、医薬品医療機器総合機構の相談窓口に寄せられた意見等について検討を行っています。必要な場合には、医薬品に関する試験検査を実施しています。
また、先発薬と後発薬の同等性を確保するため、医薬品製造業者等に対する薬事監視指導において、品質管理基準の指導(*3)や、品質確認のための試験検査が実施されています。
更に、ジェネリック医薬品品質情報検討会(*4)での検査結果等を踏まえて、品質に関する情報を体系的にまとめた医療用医薬品最新品質情報集(通称「ブルーブック」)が作成され、 同検討会のホームページ内で公表されています(*5)。
(3) 安定供給体制の整備
ジェネリック医薬品供給ガイドライン(日本製薬団体連合会)に基づいて、各後発薬メーカーが、安定供給マニュアルを作成しています。また、厚生労働省のホームページ内で、各メーカーが、安定供給体制等に関する情報などを掲載、公表しています(*6) 。
(*3) 立ち入り検査による、医薬品及び医薬部外品の製造管理および品質管理に関する基準(Good Manufacturing Practice, GMP)の指導を指します。
(*4) 国立医薬品食品衛生研究所が、厚生労働省の委託を受けて、2008年に設置しています。
(*6) アドレスは、http://www.mhlw.go.jp/seisakunitsuite/bunya/kenkou_iryou/iryou/kouhatu-iyaku/kigyou/list.html
3――医薬品メーカーの動き
近年、ジェネリックの普及を受けて、医薬品メーカーでは、関連した動きが出ています。オーソライズド・ジェネリック、医薬品メーカーのM&Aや事業売却、産学共同研究やオープン・イノベーションです。
1|オーソライズド・ジェネリックにより、新薬メーカーは対抗策を進めています
新薬メーカーにとって、後発薬への置き換えは、長期収載品の販売減を意味し、収益減につながることを意味します。
そこで、新薬メーカーは、オーソライズド・ジェネリック(AG)という対抗策を打ち出しています。これは、新薬の特許期間中に、新薬メーカーが関連会社を通じて新薬と有効成分が同じ医薬品を、新薬よりも安い価格で発売し、市場に浸透させるものです。
AGの製造会社は、先発薬の特許期間中、新薬メーカーにロイヤリティーを支払います。もし後発薬メーカーが新薬の特許期間中にAGを発売しようとしても、ロイヤリティーの支払いにより利益が出せません。従って後発薬メーカーは新薬の特許切れを待つしかありません。
しかし、新薬の特許期間後に、後発薬を発売しても、AGと価格面で大きな差が無いため、市場への浸透は見込みにくいこととなります。AGは、新薬メーカーが先手を打って後発薬市場を自社グループで囲い込む戦略なのです。
なお、AGは新薬の特許を引き継ぐため、医療機関側の心配が少なく、採用されやすいという特徴もあります。
2|医薬品メーカーのM&Aや事業売却が進んでいます
医薬品メーカーにとって、創薬を巡る環境は、厳しくなっています。各国で、高齢化が進み、社会保険の負担軽減に向けて、医療費抑制政策がとられています。
また、新薬候補の化合物が枯渇するなか、新たな創薬技術へのキャッチアップが求められるなど、研究の難度が高まっています。一方で、副作用等に関する、薬剤の安全性基準は厳格化され、臨床試験の負荷は増大しています。こうしたことを受けて、海外では、医薬品メーカーのM&Aによる合従連衡が進んでいます。
一方、国内では、後発薬に関連して、新薬メーカーが収益力を維持するために、長期収載品を他社に移管する動きが出ています。これは、「オフ・パテント・ドラッグ(特許期間を満了した医薬品製品群)」の販売戦略と呼ばれています。
長期収載品を買い取る側には、製品ポートフォリオを充実させることで、医療機関からの信頼が高まるというメリットがあります。このように、医薬品業界では、M&Aによる合従連衡や、後発薬に伴う事業売却の動きが加速しています。
3|産学共同研究やオープン・イノベーションの動きも進んでいます
医薬品メーカーと、大学や研究所等のアカデミアの産学の共同研究をする動きも活発化しています。共同研究に要する費用を確保するために、医薬品メーカーが、ベンチャーファンドを創立して、金融ファンド等から、資金を集めることも一般的となっています。
また、創薬に活かすことを目指して、医薬品メーカーが研究公募制度を設けて、研究者個人の知見を募ることも行われています。
こうした動きに対して、国は、法人税の研究開発税制(*7)で、自社の試験研究費控除とは別に、大学、国の研究機関、その他の民間企業等との共同研究や委託研究などの費用(特別試験研究費)について、一定割合を法人税から控除できる制度(*8)を設けるなど、オープン・イノベーションの動きを後押ししています。
ジェネリック医薬品とともに、引き続き、医薬品メーカーの動向にも注目していくことが求められます。
(*7) 所得の計算上損金の額に算入される試験研究費の額がある場合、その事業年度の法人税額から、試験研究費の額に税額控除割合を乗じて計算した金額を控除できる制度です。
(*8)「オープンイノベーション型」とされ、相手方が大学・国の研究機関(特別研究機関)等の場合は特別試験研究費の30%、その他の民間企業等の場合は特別試験研究費の20%が、法人税額の5% 相当額を上限に控除できます。
関連レポート
(2018年4月9日「基礎研レター」より転載)
株式会社ニッセイ基礎研究所
保険研究部 主任研究員
