私たちは、絶えず病原微生物による感染の危険にさらされている。これを防ぐ免疫システムの有効な手段の1つが、抗体(免疫グロブリン;Ig)による微生物の認識である。
一方、微生物にとっても感染・増殖は必至。抗体を切断して無力化し、免疫システムから逃れようとするものがいるのだ。
今回、大阪大学の荒瀬尚教授らの研究グループにより、抗体を切断する細菌のプロテアーゼ(タンパク質分解酵素)、およびその切断抗体と結合するヒト免疫細胞上の受容体が同定され、侵入微生物に対する新規の生体防御機構が明らかになった。
活性化レセプターのリガンドを探して
―― 荒瀬研では、病原体が免疫応答による攻撃を回避する仕組みと、それに対する宿主の感染抵抗性について研究されています。そこでポイントとなるのが、「ペア型レセプター」とよばれる受容体です。今回、解析されたのもペア型レセプターですね。まずは、ペア型レセプターについてお話しいただけますか。
平安氏: ペア型レセプターは、免疫細胞上に発現している受容体です。活性化レセプターと抑制化レセプターがあり、互いに細胞外のアミノ酸配列は非常に似ているのですが、細胞内の構造が異なり、それが機能を決定しています。
一般に、抑制化レセプターは自己抗原(他者と自分を見分けるための自分のマーカータンパク質)を認識(結合)して、自分に対する免疫応答を抑制しています。
一方、活性化レセプターは、抑制化レセプターと細胞外のアミノ酸配列が似ているにもかかわらず、自己抗原とは結合せず、リガンド(受容体に結合する分子)が不明なものが多いのです。
ただ、いくつかのウイルス由来のタンパク質が活性化レセプターに認識されるので、外部からの侵入異物を認識して免疫応答を活性化しているのではと考えられます(図1)。
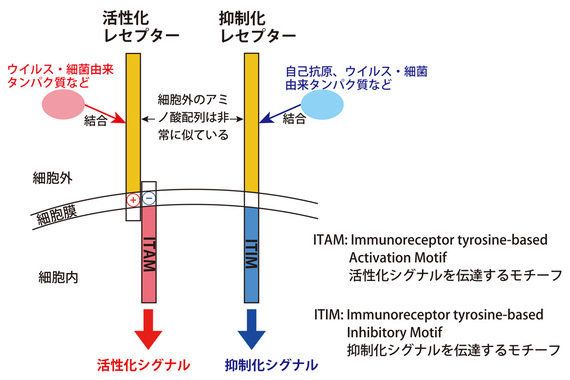
図1:ペア型レセプター
細胞外のアミノ酸配列は似ているが、細胞内は全く異なる構造になっていて、正反対のシグナルを伝達する。
荒瀬氏: 実は、抑制化レセプターは、自己抗原に対する免疫応答を抑えるだけでなく、ウイルス等の病原体が宿主分子と似た分子を用いて免疫応答を抑制するのに利用されてしまうことがあります。すると感染が起こり、人体にとって困ったことになります。そこで、似たような細胞外構造を持ち、そうした分子を認識して免疫応答を活性化する受容体を新たに進化させたのではないかと考えています。
というのも、抑制化、活性化レセプター両遺伝子は、ゲノム上では隣合わせに位置しており、おそらく遺伝子重複による産物と考えられるからです。こうした活性化レセプターを獲得できたものが、進化的に生き残ったのではないでしょうか。
ただ、獲得のきっかけがどんな病原体だったか今となってはわからないので、リガンドが不明な活性化レセプターが多いと思われます。
―― そうした活性化レセプターのリガンドの同定が、今回の研究の目的だったわけですね。これは、しらみつぶしの大変な作業だったのでは?
平安氏: はい。これまでも多くの研究者がチャレンジしてきましたが、なかなか難しいのが現状です。今回は、いろいろな種類の活性化レセプターの組み換えタンパク質を作製し、結合する分子の探索を試みました。すると、LILRA2という活性化レセプターがDaudi細胞(ヒトバーキットリンパ腫由来の細胞株)上のタンパク質と結合したのです。
一方、LILRA2の対である抑制化レセプターLILRB1には結合しませんでした。リガンドを同定したところ、抗体の一種、免疫グロブリンM(IgM)であることがわかりました。ところが、なぜか精製したIgMとは結合しません。また、別の研究室からいただいたDaudi細胞を用いると、LILRA2と結合しません。
さらに気になることに、どうも結合するIgMの分子量がちょっと小さいのです。これは何か変だと調べてみると、使用していたDaudi細胞がマイコプラズマ菌(マイコプラズマ肺炎の原因となる細胞壁を持たない小さな細菌で、真核細胞に寄生)に感染していたことがわかりました(図3a、b)。
―― つまり、予期せぬマイコプラズマ菌感染によって偶然見つかった?
平安氏: そうです。本当にラッキーでした。LILRA2は、マイコプラズマ菌によって切断され短くなったIgMを認識していたのです。切断されていたのはIgMのH鎖(図2)のアミノ末端であり、人工的にアミノ末端を切断したIgMを作製してみるとLILRA2に認識されました。
一方、全長のIgMはLILRA2に認識されませんでした(図3c)。

図2:抗体の構造
抗体は、H鎖(Heavy chain;重鎖)とL鎖(Light chain;軽鎖)2本ずつからなるY字型構造をしている。Y 字部分の約半分の領域でアミノ酸配列が異なり、抗原と特異的に結合する可変領域となっている(橙部分)。これに対して、残りのY字部分と軸の部分は定常領域と呼ばれる(緑部分)。
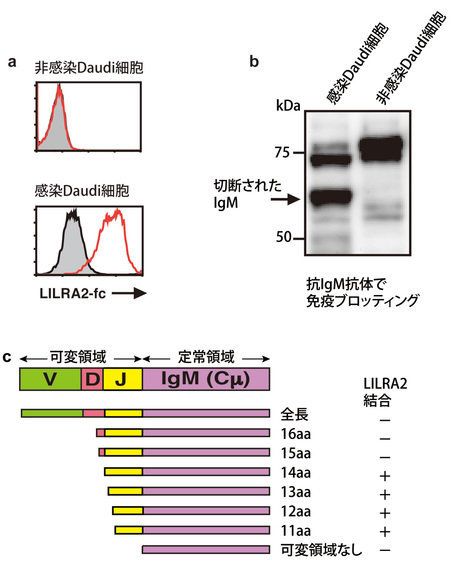
図3:LILRA2はアミノ末端が短くなったIgMと結合する
a. Daudi細胞をLILRA2-Fc融合タンパク質で免疫染色して、フローサイトメトリー解析(レーザー照射して細胞の大きさや発色などから分析する方法)すると、マイコプラズマ菌感染細胞にLILRA2と結合するタンパク質が存在した。質量分析の結果、そのタンパク質はIgMとわかった。
b. マイコプラズマ菌感染Daudi細胞のIgMは切断されていた。免疫ブロッティングは、電気泳動で分離したタンパク質を膜に転写し、抗体で検出する方法。
c. IgMの定常領域から11、12、13、14番目のアミノ酸で切断された場合、LILRA2と結合した。
―― 抗体切断は、ほかの微生物も行っているのですか。
平安氏: in vitroでは、レジオネラ菌(レジオネラ肺炎の原因細菌で、細胞内に寄生)やカンジダ(膣内や口腔内の常在真菌で、免疫機能が低下するとカンジダ症を発症)は、よくIgMを切断し、肺炎球菌(肺炎や中耳炎を引き起こす細菌)、インフルエンザ菌(インフルエンザウイルスとは異なる細菌で、肺炎や中耳炎を発症)は、弱く切断していました(図4)。
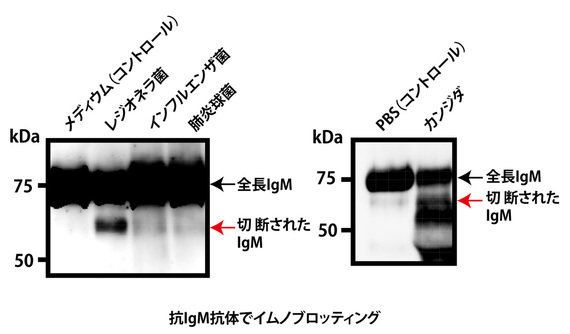
図4:さまざまな微生物が、IgMを切断する
荒瀬氏: ただ、生体内のコンディションでは、in vitroとは微生物の産生物が変わると言われており、実際には肺炎球菌やインフルエンザ菌でもよく切断されている可能性があります。
体内に侵入した微生物にとって抗体は敵ですから、それを壊して攻撃をなんとか阻止しようとするわけです。免疫の進化を考えると、LILRA2は、マイコプラズマ菌だけでなく、いろいろな病原体による抗体切断に対して反応しているのではないかと思います。
―― 微生物にとって敵である抗体の無力化に効果的なのが、アミノ末端の切断なのですね。
荒瀬氏: 抗体ヒンジ部(Y字の二股の付け根部分;図2)を切断する微生物もいますが、これでは抗体による認識を阻害することはできません。微生物も生き延びるために進化してきたのです。
平安氏: 今回の実験では、抗体を切断するプロテアーゼ(タンパク質分解酵素)を同定したのですが(後述)、このような抗体のアミノ末端を分解するプロテアーゼはこれまで同定されていませんでした。本研究が初めてです。
―― こんな風に免疫応答を抑制しようとするとは、微生物もしたたかですね。切断は、ほかの抗体にも見られ、LILRA2に認識されるのでしょうか。
平安氏: マイコプラズマ菌によってIgG1、IgG2、IgG3、IgG4が切断され、LILRA2に認識されました。IgAは、切断はされるのですが結合しませんでした。末梢血から抗体をクローニングすると、そのうちのいくつかが切断されLILRA2に認識されたことから、Daudi細胞に特異なことではなく、実際に生体内でも微生物によってさまざまな抗体が切断され、LILRA2が認識していると推察されます。
―― ほかの哺乳類にも、LILRA2のような切断抗体を認識できる受容体は見つかっているのでしょうか。
平安氏: 霊長類にはアミノ酸配列的にLILRA2に相同性のある受容体があります。マウスなどの齧歯類では、ちょっと似たアミノ酸配列のものはありますが、切断された抗体は認識しません。ただし、マウスにも機能ホモログはあるのではないかと思っています。
荒瀬氏: 実は、LILR遺伝子の隣に、NK細胞(免疫細胞の一種)上に発現するMHCクラスIという自己抗原の受容体、KIRがあります。マウスではLy49という受容体が同様の機能を持ちますが、構造は全く違います。こうしたことから、LILRA2も同じように、アミノ酸的には全く違っていても同様の機能を持つマウスホモログがあると考えられます。
平安氏: 遺伝子の祖先は違っていても、同様の環境下で独立に進化して、同じような機能を獲得したというのは非常に興味深いです。
荒瀬氏: 外来の異物と接してそれに適応しないとならない分子は進化が非常に激しいので、ヒトとマウスで保存されていないものは、こういった感染にかかわるものが多いと思います。
LILRA2からのシグナルが感染を防ぐ
―― さて、こうした微生物の巧妙な感染手段を阻止するには、受容体からのシグナルが細胞内に伝わることが重要かと思います。
平安氏: はい、そのとおりです。本研究では、LILRA2が活性化すると細胞内にシグナルが伝達されてGFP(緑色蛍光タンパク質)が発現し、細胞が光るレポーター細胞を利用して調べました。
結果、全長IgMでは活性化しないのですが、細胞にマイコプラズマ菌を感染させる、あるいはアミノ末端切断のIg Mだと細胞が光り、活性化しました。さらに、LILRA2を発現している好中球(白血球の1つ)系の細胞株を切断した抗体で刺激すると、サイトカイン(免疫細胞の情報伝達タンパク質)の1つIL-8の産生が上昇しました。
この反応は、LILRA2のノックアウト細胞株では見られず、LILRA2の導入によって回復しました。つまり、切断された抗体はLILRA2を介して、好中球を活性化すると考えられます。
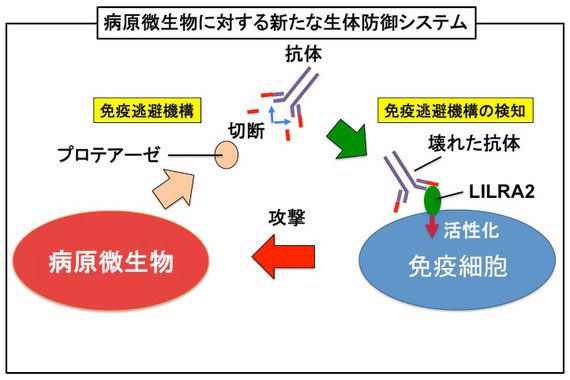
図5:今回の研究のモデル図
病原微生物は免疫システムから逃れようと抗体を切断して無力化するが、宿主は壊れた抗体をLILRA2で認識して免疫反応を活性化し、感染を阻止している。
―― ほかの白血球ではどうでしょうか。
平安氏: レジオネラ菌は、単球に感染して細胞内で増殖します。レジオネラ菌を感染させた単球のLILRA2を切断型抗体で刺激すると、菌の増殖が抑制されました。単球では細胞内の微生物の増殖が抑制される、つまり直接生体防御にかかわっているのだと思います。
―― 生体内の感染局所でも、こうした反応は見られますか。
平安氏: 中耳炎や副鼻腔炎患者さんの膿汁を調べてみました。中耳炎の膿汁には肺炎球菌やインフルエンザ菌、副鼻腔炎の膿汁には表皮ブドウ球菌(通常は表皮や鼻腔に常在して他の菌の侵入を防いでいるが、体内に侵入すると病原性を発することがある。)やアクネ菌(皮膚常在細菌で、ニキビの原因細菌の1つ)が見られ、IgM、IgGが切断されていました。
これらの切断抗体は、LILRA2のレポーター細胞を活性化することから、実際の感染局所でも抗体が切断されてLILRA2の認識機能が働いていると思われます。
抗体を切断する細菌プロテアーゼの同定
―― 今回の研究では、抗体を切断する細菌のプロテアーゼを同定しましたね。
平安氏: レジオネラ菌感染細胞より Msp(Major Secretory Protein)と呼ばれるプロテアーゼを単離しました。作製したMspの組み換えタンパク質は、確かにIgMを切断し、切断されたIgMはLILRA2のレポーター細胞(上述)を活性化しました。また、Mspを欠損させたレジオネラ菌ではIgMを切断できなくなりました。つまり、MspがIgMを切断するプロテアーゼであると考えられます。
―― レジオネラ菌以外でもMspが関与している?
平安氏: 似たようなプロテアーゼがあると思います。アミノ酸相同性の検索をかけると、緑膿菌(成人の腸内や環境中に広く存在している細菌。免疫力の低下で病原性を発する。)などに近いものが見つかってきます。
ただ、細菌のプロテアーゼは種間で独立して進化しており、こうした検索で引っかかるものが少ないのです。おそらく、マイコプラズマ菌やカンジダにも、アミノ酸配列に相同性がなくても同様の機能を持つプロテアーゼがあるのだろうと考えられます。
―― Mspはほかのタンパク質も分解するのでしょうか。
平安氏: サイトカインのIL-2を切断するという報告があります。Mspによって切断された抗体は宿主のLILRA2が認識していますが、サイトカインをはじめとするほかの免疫系タンパク質の分解では、宿主が別の受容体で認識し、免疫応答を活性化しているのかもしれません。
今後に向けて
―― 今後はどのように研究を発展させていきたいとお考えですか。
平安氏: 本研究に関していえば、マウスの機能ホモログを見つけたいですね。
荒瀬氏: 見つかればノックアウトマウスを作製することができ、さらに機能解析が進みます。
平安氏: 今回、病原微生物が自身のプロテアーゼで抗体を分解して免疫システムから逃れようとしていること、これに対抗して宿主の受容体が分解された抗体を認識し、侵入微生物の増殖を抑えたり免疫応答を活性化したりしていることがわかりました。
こうした微生物のプロテアーゼは抗体以外にもいろいろなタンパク質を分解すると考えられ、リガンドがわかっていない受容体と結合する可能性があります。そうしたものを同定し、いろいろな微生物の免疫逃避機構とそれに対抗する生体防御の仕組みを見つけたいです。
荒瀬氏: 近年、腸内細菌叢や皮膚細菌叢など、常在細菌叢と宿主の関係が注目されています。多くは細菌の代謝産物が宿主に与える影響についての研究であり、細菌のプロテアーゼの解析はほとんど行われていません。
しかし、今回の研究から、常在細菌と宿主の共生に、細菌プロテアーゼによる免疫系をはじめとするいろいろなタンパク質の分解とその認識機構が関係している可能性が十分考えられます。こうした観点から研究を進めるのもおもしろいですね。
―― 最後になります。今回、Nature Microbiology に投稿されましたが、きっかけは?
荒瀬氏: 昨年、ある会議で、Nature Microbiology の創刊を知りました。知り合いの研究者も投稿するということで興味を持ち、今回の研究テーマがジャーナル主旨に合致しているのではと思い、投稿しました。創刊直後ですので、まだ知名度が低いのが残念です。早く、もっと多くの人にジャーナルの存在を知ってもらいたいですね。
―― どうもありがとうございました。
インタビューを終えて
今回の成果を知り、生物はしたたかでしなやかだなあと改めて実感しました。免疫応答を逃れて感染しようとする微生物、一方、ヒトも別の免疫反応の経路を進化させて応戦。
微生物とヒト、お互いが相互作用して進化してきたという、たいへん興味深い研究でした。
荒瀬先生は、もの静かな印象とは裏腹に、ときどき語られる口調から研究に対しての熱い思いを感じました。一方、ちょっと、緊張気味にインタビューに応えてくださった平安先生。言葉の端々に今後の課題へ向けての強い意思を感じました。
研究室もオープンで自由な雰囲気。今後もおもしろい研究に期待が持てそうです。
聞き手:田中明美 (サイエンスライター)
Nature Microbiology 掲載論文
Letter: 微生物によって切断された免疫グロブリンは自然免疫受容体LILRA2によって感知される
Microbially cleaved immunoglobulins are sensed by the innate immune receptor LILRA2
Nature Microbiology1 : 16054 doi:10.1038/nmicrobiol.2016.54 | Published online 25 April 2016
Author Profile
荒瀬 尚(あらせ ひさし)
大阪大学微生物病研究所免疫化学分野 教授
大阪大学免疫学フロンティア研究センター免疫化学研究室 教授
1990年北海道大学医学部卒業
1994年北海道大学大学院医学研究科博士課程修了 医学博士
1994年千葉大学医学部高次機能制御研究センター遺伝子情報分野 助手
2000年カリフォルニア大学サンフランシスコ校 研究員
2002年千葉大学大学院医学研究院遺伝子制御学 助教授
2004年大阪大学微生物病研究所免疫化学分野 助教授
2006年大阪大学微生物病研究所免疫化学分野 教授(現職)
2007年大阪大学免疫学フロンティア研究センター免疫化学研究室 教授(現職)
平安 恒幸(ひらやす こうゆき)
大阪大学免疫学フロンティア研究センター免疫化学研究室 特任助教
2004年東京大学医学部健康科学・看護学科(現健康総合科学科)卒業
2009年東京大学大学院医学系研究科国際保健学専攻修了 博士(保健学)
2008年日本学術振興会特別研究員
2010年大阪大学免疫学フロンティア研究センター 特任研究員
2012年大阪大学免疫学フロンティア研究センター免疫化学研究室 特任助教(現職)
【関連URL】



