セリウム(Ce)の少々不可解な酸化還元反応性と、それを利用した多様な応用について、ペンシルベニア大学のEric J. Schelterが解説する。
Credit: INGRAM PUBLISHING/ALAMY
58番元素セリウム(Ce)は、17の希土類金属[スカンジウム(Sc)、イットリウム(Y)、およびランタン(La)からルテチウム(Lu)までの15のランタノイド]のうちの1つである。希土類(rare earth)という名前のグループに属しているにもかかわらず、Ceはかなり存在量が多く、地殻中の存在度は銅(Cu)よりもやや少ない程度だ。また、Ceは意外と現代生活に普及している。例えば、酸化セリウム(IV)(CeO;別名セリア)を含んだ水性スラリーは、マイクロエレクトロニクスデバイスのウエハーや電子ディスプレイ用ガラス基板、眼鏡レンズ、その他の光学材料表面の化学機械研磨に用いられている。セリアは表面の塩基性サイトを化学的に攻撃する性質があるため、単純な機械的研磨よりも研磨速度を高めることができるのだ。
Ceがさまざまな用途に使われているのは、4f-Ce(III)酸化状態と4f-Ce(IV)酸化状態の相互変換が可能だからである。これは希土類金属の中では独特な挙動で、こうしたCe(III/IV)の特殊な酸化還元化学のために、その酸化物は、酸素の貯蔵と放出が起こる不均一触媒反応において重要視されている。酸素が抜けた不定比組成の酸化セリウム(CeO)系は通常、高いイオン移動度を示すが、それは格子中に酸素空孔8面体を持つことが要因の1つと考えられる(参考文献1)。
酸化セリウムは、工業的に重要な水性ガスシフト反応(一酸化炭素と水蒸気から二酸化炭素と水素を生成する反応)を促進する働きがあり、この反応が含まれる固体酸化物形燃料電池にも使用されている。また、石油精製工程では、燃料製造の際にCeとLaを含むゼオライト(フォージャサイト)がクラッキング触媒として用いられており、こうした燃料の燃焼により発生する有害な排ガスは、自動車の場合、三元触媒コンバーターにおいてセリアと貴金属の働きによりNとCO、HOへと変換される。つまり炭化水素燃料は、誕生するときと寿命を終えるときの両方でCeの世話になっていることになる。他にも、セリアナノ粒子は、活性酸素種を取り込む性質があるため、抗酸化治療薬としても研究が進められている。
合成化学者にとっては、Ceは、強力な酸化剤である硝酸セリウムアンモニウム(CAN)としておなじみだろう。CANは、酸化反応の最終手段と位置付けられ、1電子酸化剤として有機・無機化学分野において幅広く用いられている。酸化セリウムの有用性については既に述べたとおりだが、これほどCeが多用されているにもかかわらず、Ce(IV)の配位化学や有機金属化学はそれほど進展していない。
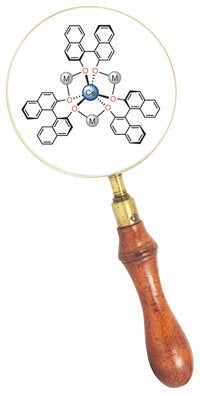
研究が進まないのは、Ce(III)配位化合物を酸化してCe(IV)生成物を高収率で単離することが意外に難しいからだと考えられる。その理由の1つに、それぞれ単一のCe陽イオンを持つ個々の錯体を合成する際には立体障害が必要であり、この立体障害が酸化反応の速度を遅めている、というものがある。我々の研究グループは最近、ヘテロバイメタリック錯体(構造式を図に示す)を用いて金属配位圏の制御を試みることにより、この問題に取り組んだ(参考文献2)。この錯体では、中心のCe原子が、リチウム(Li)陽イオンとアリールオキシド配位子が連結したフレキシブルな構造で囲まれているため、他の分子がCe原子に近づきやすく、Ce(III)は迅速かつ容易にCe(IV)へと変換された。この結果は、Ce酸化反応が速度論的に制御されるという考えを裏付けている。
Ceはその酸化還元活性ゆえに、他にも面白い性質を持つ。例えば、8回対称のエクリプス型サンドイッチ錯体セロセン(Ce(CH))などのCe化合物では、その幾分変わった電子構造が議論の的になっている。化合物中のCe陽イオンの原子価が正確にはどういった状況なのか、まだ明らかになっていないのだ(参考文献3)。エネルギー分割解析の結果は、Ce中心と各シクロオクタテトラエン環の間に強いイオン性相互作用があることを示唆しているのに対し、X線吸収分光法から得られた結果は、セロセンが多配置性の強い基底状態を持つことを示している(参考文献4)。実際、その多配置性があまりに強いため、セロセンは今や「中間原子価」を持つと表現されるほどである。つまり、この化合物中のCeは、非常に安定した開殻一重項基底状態を持ち、量子力学的に混ざり合った、Ce(III)状態とCe(IV)状態の間に位置することになる(参考文献4, 5)。
これは、一見単純に見える化合物でも、酸化状態という形式的かつ人間らしい概念では分子の本質が捉えられないという非常に興味深い例である。セロセンの4f電子の同時局在/非局在性は、f電子元素超伝導体の挙動(参考文献6)を彷彿とさせる。Ce化合物の研究が進めば、局所的挙動がどのようにエキゾチックな材料特性をもたらすかが明らかになってくるだろう。
こうした豊かな学問的探究の他にも、Ce化学を研究するための立派な現実的動機がある。Ceは、ネオジム(Nd)などの他の希土類元素とともにバストネサイトやモナザイトといった鉱物中に存在する。Ndは、風力発電機をはじめ、幅広い用途のある硬質磁性材料NdFeBをもたらす非常に価値の高い金属だが、その一般的な分離過程では、質量比でNdの3倍以上も含まれるCeが分離後に副産物として廃棄されてしまっているのである。これはまさに、Ceの新たな応用手段を探索して「Ce廃棄物」に価値を付加する、絶好のチャンスといえよう。希土類金属鉱業の利幅が薄いことを考慮すれば、なおさらだ。
Nature Chemistry5, 348(2013年4月号) | doi:10.1038/nchem.1602
doi:10.1038/nchem.1602
著者: ERIC J. SCHELTER
- Trovarelli, A. (ed.) Catalysis by Ceria and Related Materials Ch. 2, 16 (Catalytic Science Series Vol. 2, Imperial College Press, 2002).
- Robinson, J. R., Carroll, P. J., Walsh, P. J. & Schelter, E. J. Angew. Chem. Int. Ed. 51, 10159-10163 (2012).
- Edelstein, N. M. et al. J. Am. Chem. Soc.118, 13115-13116 (1996).
- Booth, C. H., Walter, M. D., Lukens, W. W. & Andersen, R. A. Phys. Rev. Lett.95, 267202 (2005).
- Kerridge, A. & Kaltsoyannis, N. C. R. Chim.13, 853-859 (2010).
- Hegger, H. Phys. Rev. Lett.84, 4986-4989 (2000).
【Nature Chemistry「In your element」で元素を楽しむ - 関連記事】
Nature Chemistry5, 804(2013年9月号) | doi:10.1038/nchem.1731
Nature Chemistry6, 166(2014年2月号) | doi:10.1038/nchem.1848
